- 주경준 기자
- 승인 2022.03.10 05:49
유럽의약품청(EMA)이 혁신적인 신약의 접근성 개선을 위해 운영중인 프라임(PRIME/PRIority MEdicines)제도 운영 5년 보고서를 최근 발표했다.
뉴스더보이스가 지난 3일 EMA 발표한 보고서 분석 결과 제도 운영 초기단계인 관계로 사실상 신속한 승인과는 거리가 먼 운영결과를 보여줬다.
보고서에 따르면 제도가 도입된 2016년 3월부터 2021년 6월까지 384건의 프라임 지정신청을 접수, 373건을 검토한 결과 95개의 후보약물을 프라임 지정했다.
이들약물중 18개 의약품이 승인됐다. 승인된 약물은 다음과 같다.
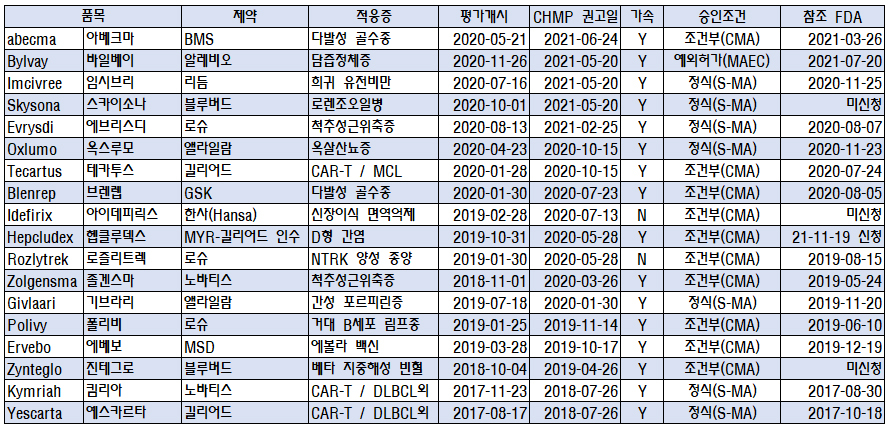
EMA가 승인한 의약품 관련 모든 활성물질의 평균 심사기간은 2020년 기준 평균 333일이다. 이와 비교 프레임 지정 의약품은 평균 310일로 차이가 크지 않았다. 또 보고서에 확인된 일부 오류를 보정하면 실제 프레임지정 의약품의 평균 심사일은 330일로 차이가 아예 없다.
일부는 6~7개월내 신속한 승인이 이뤄진 품목이 존재하는 반면 아이데피릭스가 심사기간만 최장 1년 7개월이 소요되는 등 졸겐스마, 로즐리트렉 등 심사가 1년을 훌쩍 넘기는 품목이 적잖다.
가장 최근인 BMS의 CAR-T치료제 아베크마도 1년 이상 심사기간이 소요됐으며 실제 CHMP 권고 후 EMA 승인 절차까지 포함하면 시판허가까지 1년 3개월이 걸렸다.
희귀의약품 중심으로 의학적 미충족 요구를 해결 가능성이 높은 혁신적인 신약 개발자에게 임상단계부터 최적의 지원을 제공, 신속한 승인 유도하기 위해 도입된 제도라는 점을 고려하면 신통치 않은 성과다.
한편 프라임 지정 의약품 상당수가 CAR-T 치료제 등 고가의 의약품으로 구성돼 승인된 18개 의약품의 유럽내 개별국가 판매도 부진했다.
18개 승인 약물중 유럽국가별 판매여부가 확인된 약물을 13품목. 이중 1개국 이상에서 시판되고 있는 약물은 11개 약물이며 10개국 이상에 판매되는 약물은 단 5개 품목에 불과했다.
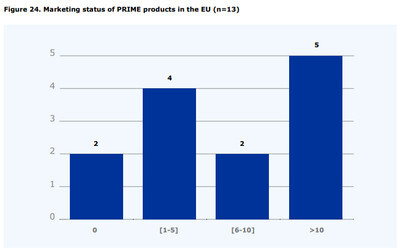
보고서는 2101년 승인된 4개약물(실제 5개) 포함 총 5개 품목의 대한 유럽내 판매(급여) 정보가 확인되지 않고 있다고 설명했다.
실제 프라임 지정 의약품으로 EMA 승인돼 유럽에서 철수된 대표적인 약물은 블루버드의 진테그로와 스카이소나 등이 있다.
이러한 이유로 EMA는 프라임 지정 의약품 제조업체는 해당 품목의 가용성을 높이기 위해 개별 국가 급여당국과의 협의 노력이 요구된다고 밝혔다.
'복불복' EMA 프라임제도...심사 최장 1년 7개월 소요 - 뉴스더보이스헬스케어 (newsthevoice.com)
'정책세상' 카테고리의 다른 글
| "감기약 쇼티지...대체조제 사후통보 면제...전문직종 피해 지원" (0) | 2022.03.23 |
|---|---|
| 약제 상한금액 재평가, '최초등재' 3170개 등 현황 공개 (0) | 2022.03.17 |
| 고가 중증희귀질환 치료제 접근성 강화...윤석열의 처방은? (0) | 2022.03.10 |
| 'FDA, 의약품 성분·부영제도 제조국·시설 모두 공개해야' (0) | 2022.03.08 |
| 약제 급여적정성 재평가 계획 공고...2년차 본평가 본격 개시 (0) | 2022.03.08 |