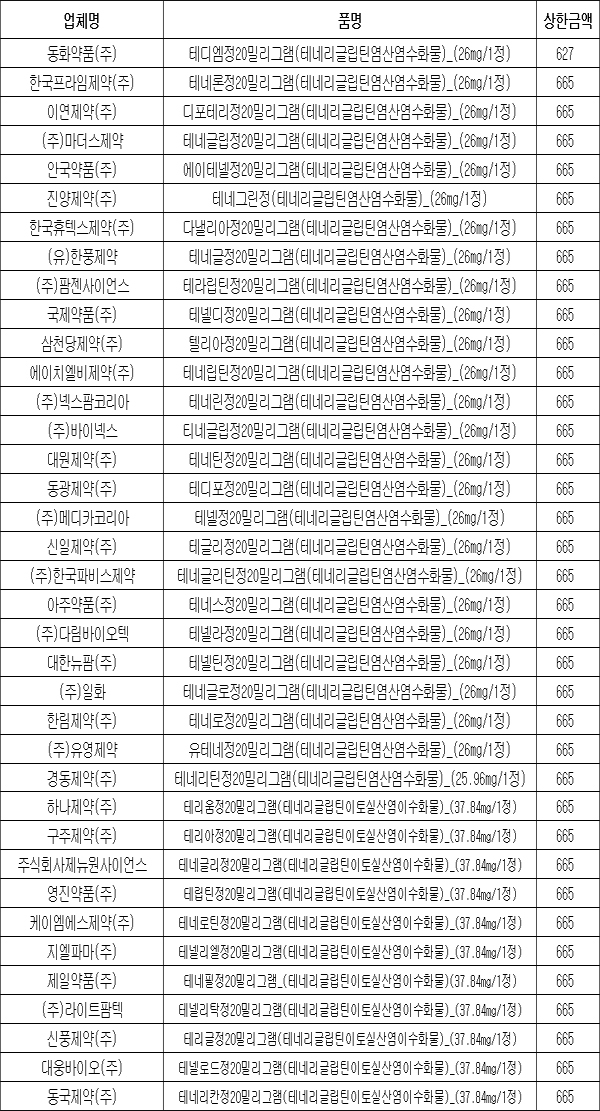
최은택 기자 승인 2022.09.26 07:55 염산염수화물 26개-이토실산염이수화물 11개 상한금액 665원...테디엠정만 627원으로 낮아 한독의 테네리글립틴 성분의 당뇨병치료제 테넬리아정과 염이 다른 개량신약이 무더기 약제목록에 등재된다. 따라서 이 성분은 10월부터 경쟁체제로 전환되게 됐다. 25일 관련 업계에 따르면 보건복지부는 이 같이 약제급여목록표 개정을 추진 중이다. 해당 품목은 모두 37개. 브롬화수소산염수화물인 오리지널 테넬리아정과 염이 다른 제품들이다. 염산염수화물의 경우 마더스제약이 제조해 업체들이 각기 허가받은 묶음의약품이다. 상한금액은 가장 낮은 가격을 선택한 동화약품의 테디엠정20mg(627원) 외에 모두 665원이다. 이는 관련 규정에 따라 오리지널인 테넬리아(739원)의 9..